Что такое co2 в химии
Углекислый газ
Углекислый газ
| Диоксид углерода | |
|---|---|
  |
|
| Другие названия | углекислый газ, углекислота, сухой лед(твердый) |
| Формула | CO2 |
| Молярная масса | 44.0095(14) г/моль |
| В твердом виде | сухой лед |
| Вид | бесцветный газ |
| Номер CAS | [124-38-9] |
| Свойства | |
| Плотность и фазовое состояние | 1.98 кг/м³, при н.у.; 771 кг/м³, жидкий; 1512 кг/м³, твёрдый |
| Растворимость в воде | 1.45 кг/м³ |
| Удельная теплота плавления | 25.13 кДж/моль |
| Точка плавления | −57 °C (216 K), под давлением |
| Точка кипения | −78 °C (195 K), возгоняется |
| Константа диссоциации кислоты (pKa) | 6.35 and 10.33 |
| Вязкость | 0.07 пз при −78 °C |
| Строение | |
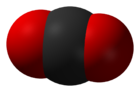
| Форма молекулы | линейная |
| Кристаллическая решётка | кварцевидная |
| Дипольный момент | ноль |
| Техника безопасности | |
| MSDS | External MSDS |
| Главные опасности | удушающее, раздражающее |
| NFPA 704 | |
| R-phrases | R: As, Fb |
| S-phrases | S9, S23, S36 (ж) |
| RTECS number | FF6400000 |
| Страница дополнительных сведений | |
| Структура и свойства | n, εr, и т. д. |
| Спектр | УФ, ИК, ЯМР, Масс-спектроскопия |
| Родственные соединения | |
| Оксиды | CO C3O2 C2O CO3 |
| Если не указано иное, данные даны для материалов при стандартных условиях (25 °C, 100 кПа) Infobox disclaimer and references |
|
Диокси́д углеро́да (двуо́кись углеро́да, углеки́слый газ, окси́д углеро́да (IV), диокси́д углеро́да, у́гольный ангидрид, углекислота́) — CO2, бесцветный газ со слегка кисловатым запахом и вкусом.
Концентрация углекислого газа в атмосфере Земли составляет 0,038 %.
Не следует путать с Диоксин.
Свойства
Физические
Плотность при нормальных условиях 1,98 г/л. При атмосферном давлении диоксид углерода не существует в жидком состоянии, переходя непосредственно из твёрдого состояния в газообразное. Твёрдый диоксид углерода называют сухим льдом. При повышенном давлении и обычных температурах углекислый газ переходит в жидкость, что используется для его хранения.
Углекислый газ легко пропускает ультрафиолетовые лучи и лучи видимой части спектра, которые поступают на Землю от Солнца и обогревают её. В то же время он поглощает испускаемые Землёй инфракрасные лучи и является одним из парниковых газов, вследствие чего принимает участие в процессе глобального потепления. Постоянный рост уровня содержания этого газа в атмосфере наблюдается с начала индустриальной эпохи.
Химические
По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует угольную кислоту. Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов. Вступает в реакции электрофильного замещения (например, с фенолом — реакция Кольбе) и нуклеофильного присоединения (например, с магнийорганическими соединениями).
Биологические
Диоксид углерода играет одну из главных ролей в живой природе, участвуя во многих процессах метаболизма живой клетки. Диоксид углерода получается в результате множества окислительных реакций у животных, и выделяется в атмосферу с дыханием. Углекислый газ атмосферы — основной источник углерода для растений. Однако, ошибкой будет утверждение, что животные только выделяют углекислый газ, а растения — только поглощают его. Растения поглощают углекислый газ в процессе фотосинтеза, а без освещения они тоже его выделяют.
Диоксид углерода не токсичен, но не поддерживает дыхание. Большая концентрация в воздухе вызывает удушье (см. Гиперкапния). Недостаток углекислого газа тоже опасен (см. Гипокапния)
Углекислый газ в организмах животных имеет и физиологическое значение, например, участвует в регуляции сосудистого тонуса (см. Артериолы).
Получение
В промышленности получают из печных газов, из продуктов разложения природных карбонатов (известняк, доломит). Смесь газов промывают раствором карбоната калия, который поглощает углекислый газ, переходя в гидрокарбонат. Раствор гидрокарбоната при нагревании разлагается, высвобождая углекислоту. При промышленном производстве закачивается в баллоны.
В лабораторных условиях небольшие количества получают взаимодействием карбонатов и гидрокарбонатов с кислотами, например мрамора с соляной кислотой.
Применение
В пищевой промышленности диоксид углерода используется как консервант и обозначается на упаковке под кодом Е290, а также в качестве разрыхлителя теста.
Жидкая углекислота (жидкая пищевая углекислота) — сжиженный углекислый газ, хранящийся под высоким давлением (
65-70 Атм). Бесцветная жидкость. При выпуске жидкой углекислоты из баллона в атмосферу часть её испаряется, а другая часть образует хлопья сухого льда.
Баллоны с жидкой углекислотой широко применяются в качестве огнетушителей и для производства газированной воды и лимонада. Углекислый газ используется в качестве активной среды при сварке проволокой так как при температуре дуги углекислота разлагается на угарный газ СО и кислород который в свою очередь и входит в заимодействие с жидким металом окисляя его. Углекислота в баллончиках применяется в пневматическом оружии и в качестве источника энергии для двигателей в авиамоделировании.
Твёрдая углекислота — сухой лёд — используется в качестве хладагента в ледниках и морозильных установках.
Методы регистрации
Измерение парциального давления углекислого газа требуется в технологических процессах, в медицинских применениях — анализ дыхательных смесей при искусственной вентиляции лёгких и в замкнутых системах жизнеобеспечения. Анализ концентрации CO2 в атмосфере используется для экологических и научных исследований, для изучения парникового эффекта.
Углекислый газ регистрируют с помощью газоанализаторов основанных на принципе инфракрасной спектроскопии и других газоизмерительных систем. Медицинский газоанализатор для регистрации содержания углекислоты в выдыхаемом воздухе называется капнограф.
Углекислый газ: характеристики и применение

Человечество научилось использовать газообразные вещества для поддержания искусственных процессов и реакций, в результате которых удаётся получить другие химические соединения. Кроме этого, различные газы используются для получения определённых физических явлений и свойств. Углекислый газ или СО2 обладает большим количеством качеств, которые не могут не использоваться в химической промышленности и быту.
Что такое углекислый газ
Оксид углерода (IV) представляет собой тяжёлый газ. Плотность углекислоты примерно в полтора раза больше чем у атмосферного воздуха. Несмотря на то, что этот газ уже при температуре минус 78,3 градуса Цельсия превращается в снегообразную массу, получить жидкую углекислоту при нормальном давлении не представляется возможным. Так называемый сухой лёд при малейшем повышении температуры сразу переходит из твёрдой, в газообразную форму. Получить жидкую углекислоту можно только при давлении более 60 атмосфер. В таких условиях газ конденсируется даже при комнатной температуре с образованием бесцветной жидкости.
Углекислый газ не окисляется, но может поддерживать горение некоторых металлов. В среде углекислоты, при определённых условиях, могут возгораться такие активные элементы как магний, кальций и барий. Этот газ хорошо растворим в воде, а в воздухе его содержится большое количество благодаря дыханию живых организмов и растений, наличию вулканической активности на земле, а также в результате сгорания органических веществ.
В результате растворения СО2 в воде в большой концентрации образуется угольная кислота. Это вещество может вступать в реакцию с фенолом и магнийорганическими соединениями. Углекислый газ также реагирует с щелочами. В результате такой реакции образуются соли и эфиры угольной кислоты.
Свойства углекислого газа
 Углекислый газ невозможно определить органами зрения или обоняния. Если концентрация СО2 невелика, то не будет ощущаться и вкуса, но при наличии большого количества этого газа в воздухе может ощущаться кисловатый привкус.
Углекислый газ невозможно определить органами зрения или обоняния. Если концентрация СО2 невелика, то не будет ощущаться и вкуса, но при наличии большого количества этого газа в воздухе может ощущаться кисловатый привкус.
При большой концентрации углекислоты во вдыхаемом воздухе может наступить отравление. Признаками негативного воздействия СО2 на организм человека являются:
- Шум и гул в ушах.
- Обильный холодный пот.
- Потеря сознания.
Учитывая тот факт, что углекислый газ тяжелее воздуха, его концентрация в нижней части помещения будет более значительной. По этой причине, первую очередь симптомы отравления могут наблюдаться у животных и детей, а также у взрослых очень маленького роста. Большая концентрация СО2 может привести к гибели людей. При потере сознания человек может оказаться на полу, где количество кислорода будет недостаточным для поддержания нормального процесса дыхания.
Углекислый газ: получение в промышленности
Существует большое количество способов промышленного получения углекислоты. Наиболее рентабельными являются варианты добычи газа, основанные на получении СО2, который образовывается на химических производствах в виде отходов.
Газообразный оксид углерода (IV) получают из промышленного дыма способом адсорбции моноэтаноламина. Частицы этого вещества подаются в трубу с отходами и вбирают в себя углекислоту. После прохождение через смесь CO2 моноэтаноламины направляются на очистку в специальные резервуары, в которых, при определённых показателях температуры и давления, происходит высвобождение углекислого газа.
Углекислый газ высокого качества получается в результате брожения сырья при изготовлении спиртных напитков. На таких производствах газообразный СО2 обрабатывают водородом, перманганатом калия и углем. В результате реакции получают жидкую форму углекислоты.
Твёрдое состояние СО2 или «сухой лёд» также получают из отходов пивоваренных заводов и ликероводочных производств. Это агрегатное состояние вещества в промышленных масштабах образуется в такой последовательности:
- Из резервуара, где происходит брожение, газ подаётся в ёмкость для промывки.
- Углекислота направляется в газгольдер, в котором подвергается воздействию повышенного давления.
- В специальных холодильниках СО2 охлаждается до определённой температуры.
- Образовавшаяся жидкость фильтруется через слой угля.
- Углекислота снова направляется в холодильник, где производится дополнительное охлаждение вещества с последующим прессованием.
Таким образом получается высококачественный «сухой лёд», который может использоваться в пищевой промышленности, растениеводстве или в быту.
Применение углекислого газа
Благодаря наличию определённых физических и химических свойств углекислый газ может использоваться в различных сферах. В химической промышленности углекислота используется для:
- Синтеза искусственных химических соединений.
- Для очистки животной и растительной ткани.
- Регулирования температуры реакций.
- Нейтрализации щёлочи.
В металлургии CO2 применяется с целью:
- Регулирования отвода воды в шахтах.
- Создания лазерного луча для резки металлов.
- Осаждения вредных газообразных веществ.
Кроме перечисленных областей углекислый газ активно используется при производстве бумаги. Оксид углерода применяется регулирования водородного показателя древесной массы, а также усиления мощности производственных машин.
Углекислый газ используется в пищевой промышленности в качестве добавки, которая оказывает консервирующее действие. При изготовлении выпечки СО2 применяется в качестве разрыхлителя. Газированные напитки также изготавливаются с применением углекислоты, а для хранения быстро портящихся продуктов используется «сухой лёд».
Незаменим углекислый газ и при выращивании овощей и фруктов в зимних теплицах. В таких помещения в воздухе недостаточное количество СО2, который необходим для «дыхания» растений, поэтому приходится искусственно насыщать атмосферу этим газом.
В медицине углекислота применяется во время проведения сложных операций на внутренних органах. Наиболее ценным качеством этого газа, является использование его для реанимационных мероприятий, ведь благодаря возможности повысить его концентрацию можно эффективно стимулировать процесс дыхания пациента.
При сварке металлов углекислота применяется в качестве инертного облака, которое служит защитой расплавленного участка от попадания в него активного кислорода. В результате такой обработки сварочный шов получается идеально ровным и не подверженным окислению.
Благодаря способности охлаждаться при испарении, СО2 используется для тушения пожаров. Заправленные этим веществом огнетушители являются эффективным средством борьбы с возгораниями на объектах, где применение порошковых или пенных средств тушения невозможно.
В быту углекислота используется в качестве напорного газа в пневматическом оружии, а также для отпугивания комаров и борьбы с грызунами.
Углекислый газ: хранение и транспортировка
Хранение СО осуществляется в баллонах чёрного цвета, на корпусе которых обязательно должна быть надпись «Углекислота».
Кроме этого, на ёмкости наносится маркировка, по которой можно получить информацию о производителе баллона, весе пустой ёмкости, а также узнать дату последнего освидетельствования. Нельзя использовать углекислотные баллоны, у которых:
- Истёк срок освидетельствования.
- Имеются повреждения.
- Неисправны вентили.
Транспортировка наполненных газом баллонов должна осуществляться по следующим правилам:
- Транспортировать ёмкости только в горизонтальном положении. Вертикальное размещение допускается только в том случае, если имеются специальные ограждения, которые препятствуют падению баллона во время перевозки.
- Для безопасного перемещения на баллонах должны быть резиновые кольца.
- Не допускать механических воздействий, а также чрезмерного нагрева.
- Запрещается перевозка углекислотных баллонов в торговых аппаратах.
Кроме этого, техникой безопасности запрещается переносить баллоны вручную или перекатывать их по земле.
Хранение баллонов с углекислотой может осуществляться как в специально оборудованных помещениях, так и под открытым небом. В зданиях ёмкости следует размещать на расстоянии не менее 1 метра от отопительных приборов. При хранении на улице необходимо оградить ёмкости от воздействия прямых солнечных лучей и осадков, поэтому размещать резервуары таким способом рекомендуется под навесом. Если хранение баллонов осуществляется в неотапливаемом помещении или под открытым небом, то в зимнее время необходимо следить за тем, чтобы ёмкости не охлаждались ниже минус 40 градусов Цельсия.
Что такое CO2


Опубликовано: 27.11.2018 Обновлено: 27.11.2018
Что такое диоксид углерода
Диоксид углерода известен в основном в своем газообразном состоянии, т.е. в качестве углекислого газа с простой химической формулой CO2. В таком виде он существует в нормальных условиях – при атмосферном давлении и «обычных» температурах. Но при повышенном давлении, свыше 5 850 кПа (таково, например, давление на морской глубине около 600 м), этот газ превращается в жидкость. А при сильном охлаждении (минус 78,5°С) он кристаллизуется и становится так называемым сухим льдом, который широко используется в торговле для хранения замороженных продуктов в рефрижераторах.
Жидкая углекислота и сухой лед получаются и применяются в человеческой деятельности, но эти формы неустойчивы и легко распадаются.
А вот газообразный диоксид углерода распространен повсюду: он выделяется в процессе дыхания животных и растений и является важной составляющей частью химического состава атмосферы и океана.
Свойства углекислого газа
Углекислый газ CO2 не имеет цвета и запаха. В обычных условиях он не имеет и вкуса. Однако при вдыхании высоких концентраций диоксида углерода можно почувствовать во рту кисловатый привкус, вызванный тем, что углекислый газ растворяется на слизистых и в слюне, образуя слабый раствор угольной кислоты.
Кстати, именно способность диоксида углерода растворяться в воде используется для изготовления газированных вод. Пузырьки лимонада – тот самый углекислый газ. Первый аппарат для насыщения воды CO2 был изобретен еще в 1770 г., а уже в 1783 г. предприимчивый швейцарец Якоб Швепп начал промышленное производство газировки (торговая марка Schweppes существует до сих пор).
Углекислый газ тяжелее воздуха в 1,5 раза, поэтому имеет тенденцию «оседать» в его нижних слоях, если помещение плохо вентилируется. Известен эффект «собачьей пещеры», где CO2 выделяется прямо из земли и накапливается на высоте около полуметра. Взрослый человек, попадая в такую пещеру, на высоте своего роста не ощущает избытка углекислого газа, а вот собаки оказываются прямо в густом слое диоксида углерода и подвергаются отравлению.
CO2 не поддерживает горение, поэтому его используют в огнетушителях и системах пожаротушения. Фокус с тушением горящей свечки содержимым якобы пустого стакана (а на самом деле – углекислым газом) основан именно на этом свойстве диоксида углерода.
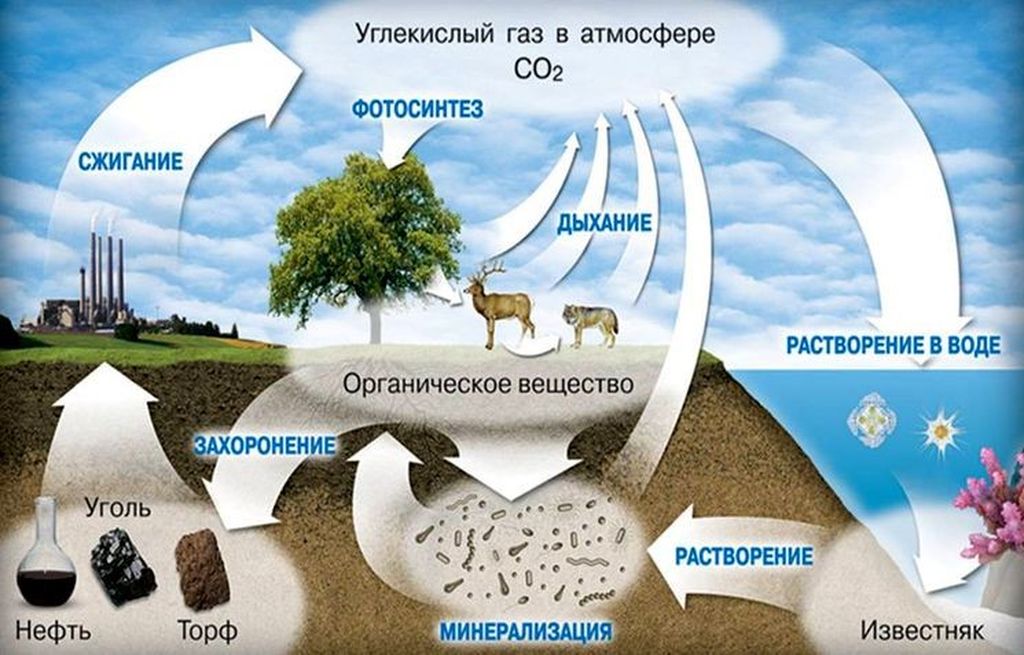
Углекислый газ в природе: естественные источники
Углекислый газ в природе образуется из различных источников:
- Дыхание животных и растений. Каждому школьнику известно, что растения поглощают углекислый газ CO2 из воздуха и используют его в процессах фотосинтеза. Некоторые хозяйки пытаются обилием комнатных растений искупить недостатки приточной вентиляции. Однако растения не только поглощают, но и выделяют углекислый газ в отсутствие света – это часть процесса дыхания. Поэтому джунгли в плохо проветриваемой спальне – не очень хорошая идея: ночью уровень CO2 будет расти еще больше.
- Вулканическая деятельность. Диоксид углерода входит в состав вулканических газов. В местностях с высокой вулканической активностью CO2 может выделяться прямо из земли – из трещин и разломов, называемых мофетами. Концентрация углекислого газа в долинах с мофетами столь высока, что многие мелкие животные, попав туда, умирают.
- Разложение органических веществ. Углекислый газ образуется при горении и гниении органики. Объемные природные выбросы диоксида углерода сопутствуют лесным пожарам.
Углекислый газ «хранится» в природе в виде углеродных соединений в полезных ископаемых: угле, нефти, торфе, известняке. Гигантские запасы CO2 содержатся в растворенном виде в мировом океане.

Выброс углекислого газа из открытого водоема может привести к лимнологической катастрофе, как это случалось, например, в 1984 и 1986 гг. в озерах Манун и Ньос в Камеруне. Оба озера образовались на месте вулканических кратеров – ныне они потухли, однако в глубине вулканическая магма все еще выделяет углекислый газ, который поднимается к водам озер и растворяется в них. В результате ряда климатических и геологических процессов концентрация углекислоты в водах превысила критическое значение. В атмосферу было выброшено огромное количество углекислого газа, который наподобие лавины спустился по горным склонам. Жертвами лимнологических катастроф на камерунских озерах стали около 1 800 человек.
Искусственные источники углекислого газа
Основными антропогенными источниками диоксида углерода являются:
- промышленные выбросы, связанные с процессами сгорания;
- автомобильный транспорт.
Несмотря на то, что доля экологичного транспорта в мире растет, подавляющая часть населения планеты еще не скоро будет иметь возможность (или желание) перейти на новые автомобили.
Активное сведение лесов в промышленных целях также ведет к повышению концентрации углекислого газа СО2 в воздухе.
Углекислый газ в организме человека
CO2 – один из конечных продуктов метаболизма (расщепления глюкозы и жиров). Он выделяется в тканях и переносится при помощи гемоглобина к легким, через которые выдыхается. В выдыхаемом человеком воздухе около 4,5% диоксида углерода (45 000 ppm) – в 60-110 раз больше, чем во вдыхаемом.
Углекислый газ играет большую роль в регуляции кровоснабжения и дыхания. Повышение уровня CO2 в крови приводит к тому, что капилляры расширяются, пропуская большее количество крови, которое доставляет к тканям кислород и выводит углекислоту.
Дыхательная система тоже стимулируется повышением содержания углекислого газа, а не нехваткой кислорода, как может показаться. В действительности нехватка кислорода долго не ощущается организмом и вполне возможна ситуация, когда в разреженном воздухе человек потеряет сознание раньше, чем почувствует нехватку воздуха. Стимулирующее свойство CO2 используется в аппаратах искусственного дыхания: там углекислый газ подмешивается к кислороду, чтобы «запустить» дыхательную систему.
Углекислый газ и мы: чем опасен СO2
Углекислый газ необходим человеческому организму так же, как кислород. Но так же, как с кислородом, переизбыток углекислого газа вредит нашему самочувствию.
Большая концентрация CO2 в воздухе приводит к интоксикации организма и вызывает состояние гиперкапнии. При гиперкапнии человек испытывает трудности с дыханием, тошноту, головную боль и может даже потерять сознание. Если содержание углекислого газа не снижается, то далее наступает черед гипоксии – кислородного голодания. Дело в том, что и углекислый газ, и кислород перемещаются по организму на одном и том же «транспорте» – гемоглобине. В норме они «путешествуют» вместе, прикрепляясь к разным местам молекулы гемоглобина. Однако повышенная концентрация углекислого газа в крови понижает способность кислорода связываться с гемоглобином. Количество кислорода в крови уменьшается и наступает гипоксия.
Такие нездоровые для организма последствия наступают при вдыхании воздуха с содержанием CO2 больше 5 000 ppm (таким может быть воздух в шахтах, например). Справедливости ради, в обычной жизни мы практически не сталкиваемся с таким воздухом. Однако и намного меньшая концентрация диоксида углерода отражается на здоровье не лучшим образом.
Согласно выводам некоторых исследований, уже 1 000 ppm CO2 вызывает у половины испытуемых утомление и головную боль. Духоту и дискомфорт многие люди начинают ощущать еще раньше. При дальнейшем повышении концентрации углекислого газа до 1 500 – 2 500 ppm критически снижается работоспособность, мозг «ленится» проявлять инициативу, обрабатывать информацию и принимать решения.
И если уровень 5 000 ppm почти невозможен в повседневной жизни, то 1 000 и даже 2 500 ppm легко могут быть частью реальности современного человека. Наш эксперимент в школе показал, что в редко проветриваемых школьных классах уровень CO2 значительную часть времени держится на отметке выше 1 500 ppm, а иногда подскакивает выше 2 000 ppm. Есть все основания предполагать, что во многих офисах и даже квартирах ситуация похожая.
Безопасным для самочувствия человека уровнем углекислого газа физиологи считают 800 ppm.
Еще одно исследование обнаружило связь между уровнем CO2 и окислительным стрессом: чем выше уровень диоксида углерода, тем больше мы страдаем от окислительного стресса, который разрушает клетки нашего организма.
Углекислый газ в атмосфере Земли
В атмосфере нашей планеты всего около 0,04% CO2 (это приблизительно 400 ppm), а совсем недавно было и того меньше: отметку в 400 ppm углекислый газ перешагнул только осенью 2016 года. Ученые связывают рост уровня CO2 в атмосфере с индустриализацией: в середине XVIII века, накануне промышленного переворота, он составлял всего около 270 ppm.

Несмотря на такое ничтожное процентное содержание диоксида углерода в атмосфере, он оказывает огромное влияние на климат планеты. Углекислый газ – один из парниковых газов. Он поглощает и удерживает инфракрасное излучение с поверхности Земли, что в конечном итоге способствует повышению температуры на планете. Этот процесс называется парниковым эффектом. Без парникового эффекта температура на земном шаре была бы примерно на 30°С ниже.
Атмосфера Венеры на 96,5% состоит из углекислого газа, и, по-видимому, тоже подвержена парниковому эффекту. Из-за него Венера является самой жаркой планетой Солнечной системы, она горячее даже ближайшего к Солнцу Меркурия. Температура на Венере около 464°С – этого хватит, чтобы расплавить свинец и олово.
Рост уровня СО2 в атмосфере Земли ведет к усилению парникового эффекта, а тот, в свою очередь – к необратимым изменениям климата. Уже сейчас можно наблюдать таяние ледников. Например, знаменитая снежная шапка Килиманджаро уменьшилась за последние 100 лет на 80%.
Заключение
Что и говорить, без углекислого газа наш мир был бы совершенно другим. Он участвует в важнейших химических, биологических, климатических и геологических процессах на Земле. И чем больше мы о них знаем, тем проще нам принимать важные решения: выбирать образ жизни и создавать свою среду – свой здоровый и комфортный микроклимат.
Все что нужно знать об углекислом газе образованному человеку
Углекислый газ содержится в воздухе в небольшом количестве, но он воздействует на человека на глубинном уровне. В статье вы найдете подробное описание химических, физических и биологических свойств газа, узнаете, где применяется в промышленности и медицине.
- Что такое углекислый газ
- Углекислый газ в атмосфере
- Углекислый газ в помещении
- Свойства углекислого газа
- Физические свойства
- Химические свойства
- Получение углекислого газа
- Природные источники углекислого газа
- Лабораторные способы получения
- Промышленные способы получения
- Применение углекислого газа
- Влияние углекислого газа на организм человека
- Синдром больного здания
- Респираторный ацидоз
- Состояние организма человека в зависимости от уровня СО2
Что такое углекислый газ
Углекислый газ («диоксид углерода», «двуокись углерода», «угольный ангидрид», carbon dioxide) – газ, являющийся частью атмосферного воздуха. Форма обозначения вещества: СО2.
Его невозможно увидеть в привычных условиях, он прозрачен и пропускает ультрафиолет и видимый спектр световых волн. При значительном давлении он переходит в жидкую форму, это возможно на глубине свыше 590 метров.
Углекислый газ является частью всех мировых процессов газообмена в атмосфере, грунте и водных бассейнах. Он входит в состав всех живых организмов, а для большинства живых организмов и растений является одним из основных функциональных компонентов дыхания как жизненно важного процесса.
Человек применяет двуокись углерода в разнообразных целях, в частности – в виде защитной среды при сварке.
Углекислый газ в атмосфере
Углекислый газ в атмосфере находится в количестве до 0,045% — или порядка 800 миллиардов тонн только в виде газа. В воде и почве его ещё больше.
Сегодня это составляет порядка 400 ppm (400 миллионных частей). Для сравнения: 300-350 лет назад, до начала Великой индустриальной революции, когда в 17 веке был начато кардинальное преобразование мировой экономики в сторону индустриализации, этот параметр составлял около 250 ppm.
Интересно, что в черте города показатель доходит до 450-470 ppm, а в публичных заведениях по типу школы – 1000-1200 и более. Это говорит о негативном влиянии транспорта и скопления людей.

Несмотря на своё крошечное количество СО2 играет значительную роль для биосферы и экологии. Основная форма влияния – воздействие в качестве парникового газа:
- газ препятствует выходу инфракрасного излучения с планеты в окружающее пространство;
- температура атмосферы год за годом увеличивается;
- происходят изменения природных явлений и климата;
- текущий формат этих преобразований – ускоренное таяние ледниковых «шапок», повышение уровня Мирового океана и изменения в составе биосферы.
Учёные рассчитали, что без присутствия этого эффекта среднегодовая температура на поверхности планеты находилась бы ниже на 25-30°С.
Углекислый газ в помещении
В помещении основным источником образования СО2 являются люди. Ежечасно взрослый человек выдыхает до 20 литров (0,5 кубометров) газа в спокойном состоянии и до 35-40 литров при значительной физической активности.
В зависимости от характера комнаты диоксид углерода может дополнительно образовываться от действия газового котла и плиты.

Средняя допустимая плотность углекислого газа для помещения – от 600 ppm, в связи с чем необходимо регулярно проветривать все жилые и технические помещения, включать соответствующие системы вентиляции или просто ненадолго открывать окна.
Углекислый газ тяжелее чистого воздуха примерно в полтора раза, поэтому он скапливается в помещениях подвального и цокольного расположения.
Свойства углекислого газа
Свойства углекислого газа таковы, что в нормальных условиях его невозможно прочувствовать. Ощущения запаха и вкуса появляются только при увеличении концентрации – проявится кисловатость во рту, вызванная образованием малого количества угольной кислоты на основе влаги слизистых оболочек.
Растворимость углекислого газа в воде и сиропах широко применяется в пищевой отрасли – для создания различных напитков.
В горении газ не участвует, что закономерно привело к его применению в современных устройствах для тушения огня (к примеру, углекислотные огнетушители). Токсичность отсутствует, остальные свойства с точки зрения безопасности человека следует оценивать аккуратно.
Физические свойства
Основные свойства у углекислого газа следующие:
- превалирующее природное агрегатное состояние: газообразное;
- возможное изменение: переход в твёрдое кристаллообразное состояние (так называемый «сухой лёд») при охлаждении до минус 78°С или жидкое состояние при давлении около 60 атмосфер;
- особые признаки по вкусу и запаху в нормальном состоянии: отсутствуют;
- восприимчивость к электричеству: проводником не является, при образовании тлеющего разряда излучает светло-зелёное свечение;
- плотность: около 1,97 грамм на литр;
- растворимость в органических веществах: частичная;
- способность к горению: отсутствует, в его окружении горят редкоземельные и щелочные металлы.
Теплопроводностью почти не обладает.
Химические свойства
Основные химические свойства у соединения такие:
- тип вещества: оксид кислотного класса (способен образовать угольную кислоту при наличии воды);
- термическое разложение: да, на кислород (О) и угарный газ (СО);
- химическая активность: взаимодействие с основаниями и оксидами активных металлов, с простыми веществами – при наличии катализатора;
- обнаружение: при прохождении СО2 через воду с лакмусом изменяет цвет в сторону красных оттенков, а известковая вода (растворенный гидроксид кальция) помутнеет;
- отношение к горению: вытеснение кислорода и остановка тления.
Данный оксид углерода имеет валентность IV: в молекуле присутствуют 2 атома кислорода, каждый из которых «оттягивает» на себя по 2 свободных электрона, в результате чего углерод оказывается «связан» кислородом.

Получение углекислого газа
Одной из основных проблем современной экологии является повсеместное образование углекислого газа в техногенной сфере: дымовые и топочные газы, продукты разнообразных химических реакций, функционирование транспорта и промышленности, строительная (производство цемента) и пищевая (брожение алкоголя) отрасли отличаются больше других.
Мировая общественность регулярно пишет о снижении выбросов carbon dioxide, но для науки и техники газ имеет значительное практичное значение.
Природные источники углекислого газа
В естественных условиях источниками углекислоты являются:
- дыхательные газообменные процессы у растений и животных: если с бактериями и млекопитающими всё понятно, то даже зелёные организмы выделяют этот газ;
- распад органических веществ на более простые продукты: в ходе химического (так называемое «естественное разложение») и термического (сгорание) преобразования образуется много СО2, и особенно много – при пожарах в лесах;
- выбросы вулканов, подземных и подводных источников: углекислый газ является компонентом выброса таких газов в большой концентрации.
Сюда также можно отнести содержание газа в различных углеродных ископаемых – от известняка до нефти. Помимо этого, его значительное количество оказалось растворённым в водах океанов и морей.
Лабораторные способы получения
Наиболее устойчивый и эффективный (по сочетанию трудозатрат и количества продукта на выходе) способ искусственного получения – работа с аппаратом Киппа.

Устройство рассчитано на создание контролируемого воздействия жидкой среды на твёрдое. В данном случае – обработка концентрированной соляной кислотой дроблёных кусков и мелкой фракции мрамора. Также будут полезны сода и обычный мел.
Для исследовательских целей быстрее всего взять готовый газ в баллонах – он чище и будет подаваться под необходимым давлением.
Промышленные способы получения
«Сырьё» для генерирования и сбора углекислого газа дают промышленные процессы и различные химические реакции при обработке ископаемых. Углекислоту возможно получать целым спектром способов:
- термическая обработка известняка: при обжиге сырьё распадается на углекислый газ и оксид кальция;
- физическое воздействие на дымовые газы: улавливаемые смеси пропускают через карбонатный раствор калия или моноэтаноламина, в результате чего образуется гидрокарбонат – при его нагреве или понижении давления воздуха вокруг него высвобождается СО2;
- пиролиз атмосферного воздуха: разделение с помощью нагрева и электрического тока на углекислоту, чистые кислород, азот, аргон и другие компоненты;
- пиролиз газовых продуктов брожения спиртов;
Об этих и некоторых других процессах снято множество видео.
Применение углекислого газа
Что такое углекислота с практической точки зрения? Это – газовая защита от окружающего воздуха и вызываемых им процессов:
- перевозка и хранение различных пищевых продуктов (полуфабрикаты, мясо, рыба), при этом наблюдается отсутствие появления плесени и гнили органики;
- внесение в напитки для придания им полезных свойств – отмечается благоприятное действие на организм газированной минеральной или сладкой воды;
- создание пищевых добавок для повышения сроков и условий хранения пищевых продуктов (к примеру, разрыхлитель Е290);
- изготовление кофе без кофеина (участвует в технологическом процессе удаления растворенного вещества);
- организация целебных ванн с углекислотой для поддержания и восстановления здоровья сердечно-сосудистой системы;
- целый спектр специализированных задач в медицине – к примеру, работа с образованиями в тканях, стимуляция дыхания;
- проверка морозоустойчивости резинотехнических изделий (в частности – автомобильные покрышки, которые испытываются с сухим льдом);
- испытания различного оборудования, механизмов и инструментов на предмет пониженных температур;
- изготовление и перезаправка углекислотных огнетушителей (наиболее эффективное средство тушения огня на электрооборудовании и горючих жидкостях);
- рабочая среда в пневматическом оружии;
- применение в качестве реагента для химических реакций с целью синтеза и производства солей, полимеров и различных волокон;
- очистка сточных вод от загрязнений;
- защита расплавленного металла сварочной ванны.

Также интересно использование для авиационного и судостроительного моделирования как вид источника энергии для двигателей с различным объёмом (до десятков см3).
Влияние углекислого газа на организм человека
Углекислый газ наравне с кислородом обеспечивает жизнь организма. Суть его работы сводится к высвобождению связанного гемоглобином кислорода – для питания тканей и отдельных органов. Для углекислоты важен в первую очередь баланс – количественное соотношение молекул СО2 и О2.
Он является для организма вазодилататором – веществом, которое влияет на состояния кровеносных сосудов, расширяя и расслабляя их. Это напрямую связано со снабжением кислородом при физической активности:
- в спокойном состоянии номинальное поперечное сечение артерии или капилляра находится в оптимальном размере;
- при необходимости приложения физической силы (спасение жизни, полезная работа) содержание углекислоты в крови несколько повышается – это регулируется вне зависимости от желания человека;
- стенки сосудов расслабляются и смягчаются из-за специфичного действия газа;
- происходит увеличение поперечного сечения сосуда, из-за чего мощность кровотока возрастает;
- как следствие повышается количество доставляемого к тканям ценного кислорода, питающего мускулатуру, что приводит к повышению физического ресурса.
Наблюдается также явление нецелевого повышения содержания углекислоты – при воспалительных процессов, при повреждении организма, проблемах с кровеносной системой вплоть до ишемии. Это чревато атипичным составом газового обмена и нуждается в регуляции силами медицины.
Несмотря на это газ всё же является компонентом «нормального» дыхания. Он переносится кровеносной системой и присутствует в плазме крови, гемоглобине и тканях. Интересно, что находится в организме он при парциальном давлении – во всём доступном пространстве, без скопления в отдельных областях.
Синдром больного здания
Этот феномен касается тех, кто продолжительное время находится в помещении. Проявляется он в неприятном самочувствии, вялости, тяжести в голове и даже заложенности носа. Интересно, что всё это очень быстро пропадает после выхода на улицу.
Суть проблемы – в повышенном содержании углекислого газа. Незаметная сложность любого здания в отношении здоровья – концентрация СО2, резко отличающаяся от нормы. Допустимые 600-800 ppm превращаются здесь в 1000-2000 ppm – это оказывает негативное и тормозящее воздействие на человека.
Решение – в вентиляции. При низком поступлении свежего воздуха содержание углекислого газа постоянно повышается – его необходимо «вымывать» проветриванием.
Респираторный ацидоз
При избытке СО2 в воздухе в организме также повышается его содержание. Это изменяет степень кислотности крови и вызывает комплекс симптомов респираторного (дыхательного) ацидоза. Это явление характеризуется повышенным сердцебиением, упадком сил, беспокойством и сниженным порогом концентрации умственных возможностей. Наиболее критична потеря сознания.
При кратковременном нахождении в «зараженной» углекислым газом атмосфере негативные симптомы проходят при обновлении воздуха или по выходу на улицу. Хуже, если пребывать в таких условиях постоянно: развивается ацидоз хронический. При нём снижается уровень иммунитета, развиваются заболевания дыхательной и сердечно-сосудистой систем, нарушается сон, ухудшается уровень физических возможностей человека.
Суть явления – в изменении кислотно-щелочного баланса крови, измеряющегося в pH.
Состояние организма человека в зависимости от уровня СО2
«Химия» организма интересна двойственным поведением ко всем веществам. Углекислота – не исключение: в привычных, естественных, дозах она является необходимой, а при превышении концентрации в окружающем воздухе оказывается токсичной и способна вызвать смерть живого организма.
Так называемая гиперкапния (состояние, вызываемое при перенасыщении организма углекислым газом) характеризуется наличием головной боли, затруднением дыхания и необходимостью его поддержания волевыми усилиями, тошнотой и потерей сознания.
Следующая стадия – гипоксия: заметное снижение количества кислорода, критически необходимого для дыхания. Оба газа транспортируются по организму одним способом, с помощью гемоглобина. Поэтому пониженное содержание кислорода мгновенно сказывается на функционировании почти каждой клетки, что приводит к существенному ухудшению самочувствия и физических возможностей.

Эти симптомы возникают при существенной концентрации углекислоты – на уровне тысяч ppm. Но уже при одной тысяче ppm возникают переутомление и даже головная боль, подкрепляемые ощущением духоты. При двух тысячах ppm работоспособность заметно падает.
Физиологи резюмируют: высокое содержание углекислого газа в воздухе напрямую влияет на разрушающие процессы окисления, происходящие в организме.



